1. Introducción
Gracias al desarrollo de la tecnología, la medicina moderna tiene a su disposición una gran cantidad de información acerca del estado del cuerpo humano. Diferentes medidas biológicas como por ejemplo presión, temperatura, concentración química o potenciales bioeléctricos resultan de gran utilidad para comprobar el estado normal o anormal de la condición física de los pacientes.
Los potenciales bioeléctricos (o biopotenciales) son producidos como resultado de la actividad electroquímica de una cierta clase de células, conocidas como células excitables, que componen los tejidos nervioso, musculares y glandulares, y presentan un potencial de acción cuando son estimuladas. Estas señales eléctricas son recogidas en forma de diferencia de potencial por los equipos de medición, que los convierten en señales e indicadores que pueden ser de utilidad para el personal médico.
Existen diferentes técnicas que hacen uso de estas medidas biológicas, tales como la electrocardiografía (ECG), electromiografía (EMG), electrorretinografía (ERG), electroneurografía (ENG) o electroencefalografía (EEG).
La electroencefalografía puede ser definida como la técnica médica que recoge actividad eléctrica generada por las estructuras del cerebro. Debido a su capacidad para reflejar la actividad del cerebro, se considera una herramienta muy poderosa en el campo de la neurología y la neurofisiología clínica.
La existencia de corrientes eléctricas en el cerebro fue descubierta en 1875 por el fisiólogo británico Richard Caton. El psiquiatra alemán Hans Berger fue el primero que analizó de manera sistemática la actividad cerebral en 1924, e introdujo el término electroencefalograma para denominar a las fluctuaciones de potencial de las señales recogidas del cerebro. La actividad que observó cambiaba de acuerdo al estado funcional del cerebro (sueño, anestesia, falta de oxígeno o epilepsia), lo cual fue corroborado por estudios posteriores.
En la actualidad, el empleo de la tecnología EEG ha traspasado el ámbito médico del diagnóstico con la proliferación de los sistemas BCI (Brain Computer Interface), que permiten una comunicación directa entre el cerebro y un dispositivo externo. Estos dispositivos presentan una gran utilidad en campos como la asistencia o reparación de las funciones motoras o sensoriales, con aplicaciones interesantes en control de prótesis, rehabilitación e interfaces de usuario [1].
Las técnicas BCI pueden ser clasificadas en dos grupos principales:
- Implantable: Situado directamente en el cerebro mediante neurocirugía. Este tipo de sistemas hace uso de miles de electrodos localizados en un pequeño circuito integrado (IC). La literatura científica ofrece gran cantidad de trabajos que acometen el diseño e implementación de estos dispositivos, los cuales presentan fuertes restricciones en superficie de implementación y consumo energético [2]. Aunque estos sistemas permiten obtener una gran calidad en las señales, el uso de esta tecnología es muy limitado debido a la necesidad de técnicas quirúrgicas y sus potenciales riesgos derivados del uso a largo plazo.
- No invasiva: Este tipo de técnicas recoge la actividad cerebral sin realizar intervención quirúrgica sobre el sujeto, a través de electrodos que se colocan en el cuero cabelludo. El uso de este tipo de dispositivos es preferible debido a su facilidad de utilización, portabilidad, y menor coste. Sin embargo, las medidas obtenidas a través de estos sistemas carecen de resolución espacial y sufren efectos perniciosos de ruido [1]. En los últimos años, el diseño de sistemas ha hecho posible integrar los sensores en dispositivos de adquisición portátiles que pueden ser acomodados en gorros, bandas y cascos. El electroencefalograma se enmarca dentro de este último grupo, y se ha convertido en el enfoque más utilizado por sistemas BCI debido a su utilidad y fiabilidad [3].
2. Aplicaciones
Dentro del ámbito clínico, las técnicas EEG pueden usarse con fines diagnósticos para monitorización de alerta, localizar áreas de daño cerebral, investigar epilepsia o estudiar trastornos del sueño.
Una tendencia más reciente derivada de la aplicación del EEG en el área médica es el llamado neurofeedback, que se define como la inducción de diferentes estados de la mente mediante entrenamiento de las ondas cerebrales dentro de bandas de frecuencia deseadas [4]. El neurofeedback proporciona a los usuarios el potencial para ajustar sus propias funciones cerebrales con el fin de obtener un estado concreto con respecto a un estímulo externo, siendo una técnica de gran utilidad, por ejemplo, en rehabilitación.
Las aplicaciones de los dispositivos BCI no sólo se centran en usos clínicos y de investigación. Existen varios ejemplos comerciales del uso de esta tecnología para dispositivos portátiles de entretenimiento: Emotiv, StarLab, [5] o ENOBIO, incluyendo trabajos para control de videojuegos [3]. En [6] se presenta un trabajo en el que se recoge el estado emocional de un sujeto a través de EEG y mediante un entorno de realidad virtual, se somete a un proceso de entrenamiento de mindfulness. El empleo de este tipo de técnicas se conoce como gamificación.
La robótica industrial es otro campo de aplicación interesante para este tipo de dispositivos, donde se pueden emplear para guiar robots que llevan a cabo tareas de gran precisión y fiabilidad con la única ayuda del pensamiento humano. Estas técnicas se han probado con éxito en brazos robóticos, robots humanoides y cirugía robótica [1].
3. ¿Cómo funciona un dispositivo EEG?
Recordemos que la función de un dispositivo EEG es la extracción de energía del cuerpo humano con el fin de medir una cierta unidad biométrica (biopotenciales provenientes de la actividad cerebral), para transformarla en información potencialmente interpretable.
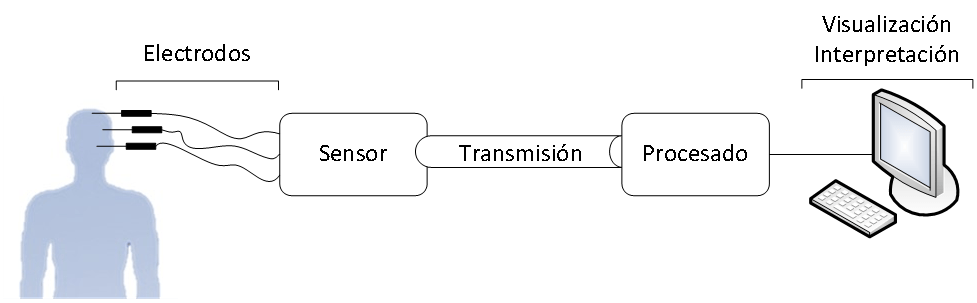
Típicamente, un sistema de adquisición de datos EEG precisa de las etapas reflejadas en la Figura 1, y que se exponen a continuación [4].
- Electrodos
Los electrodos realizan la función de interfaz entre el cuerpo y los aparatos de medida, permitiendo la conducción de la corriente eléctrica desde el cuerpo humano hasta el circuito electrónico.
Típicamente, la medida de la diferencia de potencial se realiza entre el electrodo activo (que recoge la señal) y un electrodo de referencia. Adicionalmente, suele haber un tercer electrodo (tierra) que es necesario para reducir la tensión de modo común entre el par diferencial, minimizando las interferencias [4]. En los sistemas EEG, los electrodos de referencia y modo común se localizan en la cabeza con el fin de minimizar el ruido. La localización de estos elementos en el cuero cabelludo está estandarizado siguiendo el sistema internacional de localización de electrodos 10-20.
Los electrodos pueden dividirse en dos tipos. El primero de ellos es el de los llamados electrodos húmedos, normalmente desechables pre-gelificados, o electrodos de aguja. Representan el grupo más utilizado debido a la calidad de las medidas recogidas, pero presentan el inconveniente de requerir preparación cutánea y resultan incómodos para el usuario. Además, la repetición en la toma de medidas produce una degradación del contacto entre la piel y el electrodo. El segundo grupo está formado por los electrodos secos, que evitan estos problemas, aunque la calidad de las señales es inferior y se suele emplear mayoritariamente en zonas sin pelo.
El contacto que se produce entre el cuerpo humano y la superficie de cada uno de los electrodos no es ideal, y la impedancia en esta interfaz es vista por el sensor posterior (ver la Figura 1) como una resistencia en serie conectada a los electrodos diferenciales [7]. Una baja impedancia de contacto es de vital importancia para asegurar la calidad de las medidas obtenidas, de modo que se reduzcan el ruido térmico, que se inyecta junto con la señal deseada, y las interferencias provenientes de la línea eléctrica. Con el fin de prevenir esta distorsión, la impedancia de contacto debe ser tan baja como sea posible, y siempre inferior a 5kΩ según la literatura científica [4].
Por lo tanto, comprobar la corrección de este contacto antes de adquirir los datos es un aspecto clave dentro de un sistema EEG para validar las medidas obtenidas, y por ello los sistemas comerciales disponen de recursos para medir dicha impedancia.
Esta medida normalmente se lleva a cabo inyectando una corriente a través de la interfaz electrodo-tejido y midiendo la diferencia de tensión producida entre los puntos de contacto. Este método presenta varios problemas. En primer lugar, la aplicación de una corriente activa en el paciente está restringida debido a la normativa de dispositivos médicos, y la implementación de este tipo de procesos implica un laborioso proceso de validación para el dispositivo. Un segundo inconveniente de este método es el consumo de energía, que afecta sobre todo a los sistemas autónomos con baterías. Un problema adicional es la abrasión de la piel que se produce cuando las medidas son constantes y repetitivas, lo que requiere acondicionamiento de la piel o la recolocación del electrodo tras un cierto tiempo.
Los sistemas EEG modernos son capaces de monitorizar desde 128 a 256 electrodos [8] [9], aunque el desarrollo de la tecnología permite que el número de canales monitorizados simultáneamente vaya en aumento [10].
- Sensores
Un sensor transforma una medida física en una salida eléctrica. Idealmente, el sensor debería interaccionar con el sistema vivo de manera que se minimice tanto la energía extraída como el carácter invasivo del dispositivo.
En este caso, las funciones principales del sensor son amplificar y filtrar la señal, con el fin de extraer información útil de los biopotenciales registrados. Para poder diseñar correctamente un circuito de adquisición, es necesario conocer las características de las señales que se desean interpretar, tal y como se muestra en la Figura 2.
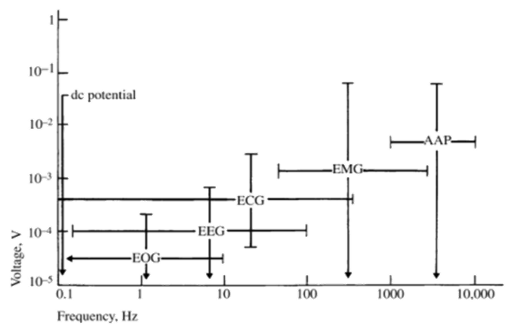
Figura 2. Rangos típicos de señales biológicas [7].
Los valores de amplitud de estas señales varían entre los 0,5 y los 100µV. Sin embargo, condiciones epilépticas producen picos de hasta 1.000 µV [4]. Debido a estas características, [4] propone unos rangos de operación para un sistema de adquisición de un dispositivo EEG.
Respecto a la ganancia del amplificador que incorpora el sensor, ésta debería estar entre 100 y 100.000 V/V, presentando una alta impedancia de entrada para evitar la distorsión de la señal.
Por otro lado, la frecuencia de muestreo del dispositivo, dadas las características de las ondas de interés, debería estar entre 128 y 1.024 Hz. Sin embargo, es común encontrar equipos con frecuencias de muestreo por encima de 1kHz, tal y como se refleja en [8].
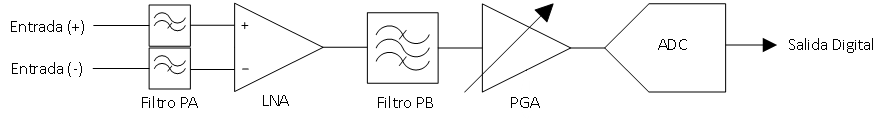
Para reunir estas características, es necesario diseñar una etapa de adquisición en el sensor, conocida como front end analógico, cuya estructura consiste en un amplificador de instrumentación de bajo ruido con ganancia fija (LNA, low noise amplifier), seguido de un PGA o VGA (programable/variable gain amplifier). Con el fin de limitar el ruido y evitar la amplificación de corriente directa, se incluyen un filtro paso alto y un filtro paso bajo en el camino de la señal [11].
Debido al tratamiento posterior de la información, a las funciones de amplificación y filtrado comentadas se debe sumar la de conversión de la señal analógica a digital, lo cual se realiza en la última etapa, conectado un ADC (analog to digital converter) a la salida del PGA. Según [8], la mayoría de unidades EEG comerciales emplean un ADC con al menos 16 bits de conversión.
La literatura científica es abundante con respecto a amplificadores de señales biológicas de bajo ruido y bajo consumo de energía, la mayoría de ellos orientado al desarrollo de circuitos integrados para dispositivos implantables [12], [13], [14], [15].
- Medio de transmisión
Una vez que la señal analógica es convertida a digital, la tecnología de transmisión (ver la Figura 1) de ésta se puede clasificar en dos categorías: cableada o inalámbrica. Actualmente, la mayoría de los sistemas existentes se construyen con conexiones cableadas, lo que da como resultado un dispositivo limitante que no resulta práctico para el uso cotidiano. El empleo de transmisión inalámbrica puede eliminar esta limitación y ofrecer una solución más ergonómica y flexible [9]. Esta tecnología es utilizada tanto en dispositivos implantables [16], [17] como en no-invasivos [18].
La mayoría de dispositivos EEG inalámbricos que se pueden encontrar en la literatura hacen uso de enlaces de comunicación basados en protocolos Bluetooth o Zigbee, o directamente en RF (radiofrecuencia). El mayor problema del Bluetooth es su pesado stack y su consumo de energía, aunque su compatibilidad permite su uso con dispositivos cotidianos como un teléfono móvil que actúe como receptor de datos [18].
La transmisión Zigbee y mediante RF, al contrario, presentan una mayor eficiencia, aunque carecen de la amplia compatibilidad del Bluetooth. Desde el punto de vista técnico y económico, esto implica un mayor esfuerzo en el desarrollo de un receptor específico.
Los sistemas de adquisición EEG están diseñados para un bajo consumo y un bajo coste. Dada la gran cantidad de información que es necesario transmitir en sistemas multicanal (con hasta 256 electrodos y altas tasas de muestreo), es posible emplear técnicas de compresión de datos o modulación digital para reducir la tasa de datos [5]. La literatura científica ofrece algunos ejemplos en esta línea. [8] presenta un estudio del balance sobre el consumo de energía entre la complejidad de un algoritmo de compresión y la reducción en la tasa de datos. [19] presenta un algoritmo de compresión de datos sin pérdida implementado en un circuito integrado.
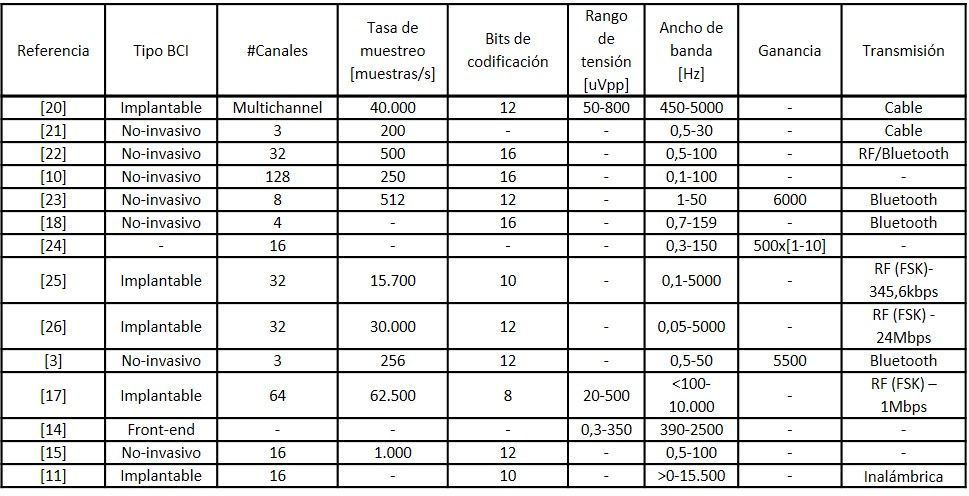
En la Tabla I se recogen algunas características técnicas de la cadena de adquisición de datos de sistemas propuestos o analizados en la literatura. Como se puede observar, la tasa de muestreo y ancho de banda presentan una gran variabilidad entre dispositivos implantables y no invasivos. El sistema presentado en [17] presenta el valor más alto de los dos tipos, pero la resolución de la señal está limitada a 8 bits, y la transmisión propuesta con RF requiere el uso de técnicas de modulación digital.
- Procesado
En la última etapa de adquisición EEG, es necesario disponer de un dispositivo que realice las funciones de recepción, procesado y representación de los resultados. Esta etapa suele incluir un acondicionamiento software de la señal y una interfaz gráfica de usuario, que muestra por pantalla las señales recogidas y permite la configuración del sensor.
Debido al reciente incremento en la complejidad de los sistemas EEG y en la cantidad de información que se registra, capturada en tiempo real, se pueden encontrar aplicaciones que hacen uso de técnicas de minería de datos [27] y algoritmos sofisticados de procesado de señal. Estas técnicas resultan especialmente útiles en el uso de dispositivos implantables, donde la cantidad de información recogida es muy amplia y es necesario decodificarla mediante algoritmos de procesamiento que incluyen técnicas de big data [28]
4. Dispositivos BCI en el ámbito médico. Problemática actual y desarrollo propuesto
La principal aplicación de estos dispositivos es el ámbito médico. Como se expondrá más adelante, los equipos comerciales actuales presentan una serie de limitaciones causadas por el empleo de tecnología cableada. Debido a ello, en el IIT se está desarrollando actualmente un trabajo de investigación que incluye una tesis doctoral, cuyo objetivo es el diseño y prototipado de un equipo de monitorización neurológica, que permita la utilización de un enlace de comunicación inalámbrico, y que cumpla con los requisitos de los equipos médicos comerciales actuales. Este prototipo consiste en el desarrollo tanto hardware como software de un dispositivo transmisor y uno receptor. Debido a su carácter innovador, el objetivo final del proyecto es obtener un equipo comercial cuya patente está en trámite actualmente. Una solución novedosa, como la que se pretende implementar, supone un avance que permitirá superar los siguientes problemas, presentes en los equipos actuales:
En primer lugar, la ergonomía. La realización de una intervención quirúrgica que conlleve monitorización neurológica (MNIO, Monitorización Neurofisológica Intraoperatoria), requiere la utilización de gran cantidad de cables que permitan la conexión de los electrodos dispuestos sobre el paciente con el receptor final, que típicamente se trata de una estación con un ordenador personal que debe estar dentro del quirófano. Esta gran cantidad de cables puede interferir con el campo estéril necesario en la intervención, así como limitar o dificultar la labor del personal médico presente en el quirófano.
En segundo lugar, la localización. El empleo de una solución cableada requiere que haya una estación en cada uno de los quirófanos en los que se realiza una intervención de este tipo, de tal forma que la toma de medidas neurológicas sólo se puede realizar de manera local.
En tercer lugar, el coste del personal. Adicionalmente a los inconvenientes expuestos anteriormente, el empleo de un dispositivo cableado implica que las medidas locales tomadas en un quirófano únicamente puedan ser leídas e interpretadas por un neurofisiólogo que esté presente en el mismo. Esta necesidad puede desembocar en dos problemas: o bien se dispone de un neurofisiólogo por cada uno de los quirófanos donde se realicen intervenciones de manera simultánea, con el consiguiente aumento del coste, o bien existe la posibilidad de que se disponga de un número más reducido de especialistas que atiendan las demandas de cada uno de los quirófanos, lo que puede generar retrasos en las intervenciones, o peor aún, que el paciente sufra las consecuencias de falta de monitorización en un momento dado.
La aplicación de tecnología inalámbrica en este ámbito permitirá resolver estos problemas, ya que se podrá hacer uso de un enlace de comunicación que, además de prescindir de gran cantidad de cables, posibilitará la deslocalización de la información. Esta información podrá transmitirse fuera incluso del quirófano, permitiendo que exista uno o varios equipos externos desde donde se realice la monitorización simultánea por parte de un único especialista de manera continua.
En la actualidad, las soluciones inalámbricas están restringidas a tecnologías implantables [26], [27], sistemas de entretenimiento [5] o bien presentan características de ancho de banda y tasas de muestreo por debajo de las requeridas en soluciones médicas. Por lo tanto, el desarrollo propuesto, denominado Wireless Intraoperative Neuromonitoring (WIONM) supone un avance cualitativo importante en la industria.
5. Agradecimientos
Los autores agradecen el soporte de Soinde S.L. (promotora del proyecto), y de la Asociación Nacional de Ingenieros del ICAI, que hacen posible la realización de este trabajo de investigación.
Bibliografía
[1] B. Zhang, J. Wang, and T. Fuhlbrigge, “A Review of the Comercial Brain-Computer Interface Technology from Perspective of Industrial Robotics,” in Automation and Logistics (ICAL), 2010 IEEE International Conference on, 2010, pp. 379–384.
[2] R. R. Harrison, P. T. Watkins, S. Member, R. J. Kier, S. Member, R. O. Lovejoy, D. J. Black, S. Member, B. Greger, and F. Solzbacher, “A Low-Power Integrated Circuit for a Wireless 100-Electrode Neural Recording System,” vol. 42, no. 1, pp. 123–133, 2007.
[3] L.-D. Liao, C.-Y. Chen, I.-J. Wang, S.-F. Chen, S.-Y. Li, B. Chen, J.-Y. Chang, and C.-T. Lin, “Gaming control using a wearable and wireless EEG-based brain-computer interface device with novel dry foam-based sensors,” J. Neuroeng. Rehabil., vol. 9, no. January, 2012.
[4] M. Teplan, “Fundamentals of EEG Measurement,” Meas. Sci. Rev., vol. 2, pp. 1–11, 2002.
[5] B. L. Liao, C. Lin, K. McDowell, A. E. Wickednden, K. Gramann, T. Jung, L. Ko, and J.-Y. Chang, “Biosensor Technologies for Augmented Brain-Computer Interfaces in the Next Decades,” Proc. IEEE, vol. 100, no. Special Centennial Issue, pp. 1553–1566, 2012.
[6] A. Choo and A. May, “Virtual Reality and Electroencephalography for Health Gamification,” in IEEE Games Media Entertainment, 2014, pp. 1–3.
[7] J. G. Webster, Medical Instrumentation: Application and Design, 4th ed. Wiley.
[8] A. J. Casson, D. C. Yates, S. J. M. Smith, J. S. Duncan, and E. Rodriguez-villegas, “Wereable Electroenchepalography,” IEEE Eng. Med. Biol. Mag., vol. 29, no. 3, pp. 44–56, 2010.
[9] R. a Andersen, S. Musallam, and B. Pesaran, “Selecting the Signals for a Brain-Machine Interface,” Curr. Opin. Neurobiol., vol. 14, no. 6, pp. 720–6, Dec. 2004.
[10] T. C. Ferree, P. Luu, G. S. Russell, and D. M. Tucker, “Scalp electrode impedance , infection risk , and EEG data quality,” vol. 112, pp. 536–544, 2001.
[11] N. Heidmann, N. Hellwege, T. Hohlein, T. Westphal, D. Peters-Drolshagen, and S. Paul, “Modeling of an Analog Recording System Design for ECoG and AP Signals,” in Design, Automation and Test in Europe Conference and Exhibition (DATE), 2014, pp. 1–6.
[12] R. R. Harrison and C. Charles, “A Low-Power Low-Noise CMOS Amplifier for Neural Recording Applications,” IEEE J. Solid-State Circuits, vol. 38, no. 6, pp. 958–965, 2003.
[13] C. Huang, S. Hung, J. Chung, L.-D. Van, and C. Lin, “Front-End Amplifier of Low-Noise and Tunable BW / Gain for Portable Biomedical Signal Acquisition,” in Circuits and Systems, IEEE International Symposium on, 2008, pp. 2717–2720.
[14] R. F. Yazicioglu, P. Merken, R. Puers, and C. Van Hoof, “A 60µW 60 nV/ √ Hz Readout Front-End for Portable Biopotential Acquisition Systems,” Solid-State Circuits, IEEE J., vol. 42, no. 5, pp. 1100–1110, 2007.
[15] J. Xu, B. Busze, H. Kim, K. Makinwa, C. Van Hoof, and R. F. Yazicioglu, “A 60nV / √ Hz 15-Channel Digital Active Electrode System for Portable Biopotential Signal Acquisition,” Solid-State Circuits Conf. Dig. Tech. Pap. (ISSCC), 2014 IEEE Int., pp. 424–426, 2014.
[16] N. M. Neihart and R. R. Harrison, “Micropower Circuits for Bidirectional Wireless Telemetry in Neural Recording Applications,” Biomed. Eng. IEEE Trans., vol. 52, no. 11, pp. 1950–1959, 2005.
[17] A. M. Sodagar, K. D. Wise, and K. Najafi, “A Wireless Implantable Microsystem for Multichannel Neural Recording,” Microw. Theroy Tech. IEEE Trans., vol. 57, no. 10, pp. 2565–2573, 2009.
[18] Y. M. Chi and G. Cauwenberghs, “Wireless Non-contact EEG/ECG Electrodes for Body Sensor Networks,” in Body Sensor Networks, International Conference on, 2010, pp. 297–301.
[19] E. Chua and W. Fang, “Mixed Bio-Signal Lossless Data Compressor for Portable Brain-Heart Monitoring Systems,” Consum. Electron. IEEE Trans., vol. 57, no. 1, pp. 267–273, 2011.
[20] R. J. Vetter, J. C. Williams, J. F. Hetke, E. A. Nunamaker, and D. R. Kipke, “Chronic Neural Recording Using Silicon-Substrate Microelectrode Arrays Implanted in Cerebral Cortex,” Biomed. Eng. IEEE Trans., vol. 51, no. 6, pp. 896–904, 2004.
[21] G. R. Müller-Putz, R. Scherer, C. Neuper, and G. Pfurtscheller, “Steady-State Somatosensory Evoked Potentials : Suitable Brain Signals for Brain – Computer Interfaces ?,” Neural Syst. Rehabil. Eng. IEEE Trans., vol. 14, no. 1, pp. 30–37, 2006.
[22] C. Lin, L. Ko, J. Chiou, J. Duann, R. Huang, S. Liang, T. Chiu, and T. Jung, “Noninvasive Neural Prostheses Using Mobile and Wireless EEG,” Proc. IEEE, vol. 96, no. 7, pp. 1167–1183, 2008.
[23] C. Lin, L. Ko, C. Chang, and Y. Wang, “Wearable and Wireless Brain-Computer Interface and Its Applications,” pp. 741–748.
[24] R. Martins, S. Selberherr, and F. Vaz, “A CMOS IC for Portable EEG Acquisition Systems,” pp. 1406–1410, 1998.
[25] C. A. Chestek, V. Gilja, P. Nuyujukian, R. J. Kier, F. Solzbacher, S. I. Ryu, R. R. Harrison, and K. V Shenoy, “HermesC : Low-Power Wireless Neural Recording System for Freely Moving Primates,” Neural Syst. Rehabil. Eng. IEEE Trans., vol. 17, no. 4, pp. 330–338, 2009.
[26] H. Miranda, V. Gilja, C. A. Chestek, K. V Shenoy, and T. H. Meng, “HermesD : A High-Rate Long-Range Wireless Transmission System for Simultaneous Multichannel Neural Recording Applications,” Biomed. Circuits Syst. IEEE Trans., vol. 4, no. 3, pp. 181–191, 2010.
[27] B. S. Makeig, C. Kothe, T. Mullen, N. Bigdely-shamlo, Z. Zhang, and K. Kreutz-Delgado, “Evolving Signal Processing for Brain–Computer Interfaces,” Proc. IEEE, vol. 100, no. Special Centennial Issue, pp. 1567–1584, 2012.
[28] D. A. Friedenberg, C. E. Bouton, N. V Annetta, N. Skomrock, M. Zhang, M. Schwemmer, M. A. Bockbrader, W. J. Mysiw, A. R. Rezai, H. S. Bresler, and G. Sharma, “Big Data Challenges in Decoding Cortical Activity in a Human with Quadriplegia to Inform a Brain Computer Interface,” in 38th Annual International Conference of the IEEE Engineering in Medicine and Biology Society (EMBC), 2016, pp. 3084–3087.